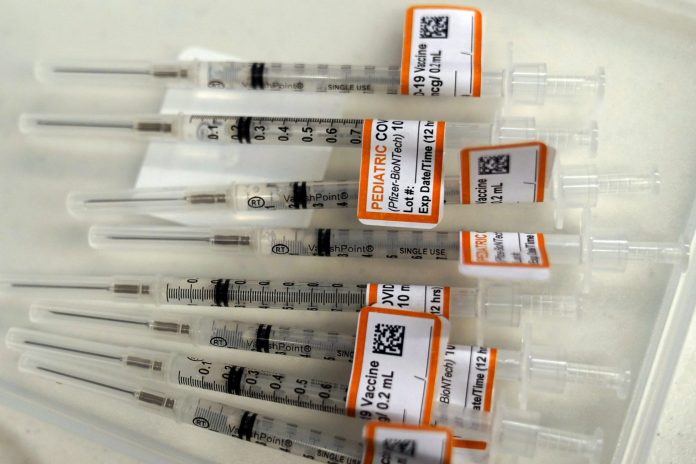
Novos dados foram enviados pela farmacêutica e, por isso, a agência reguladora adiou a decisão sobre o assunto, que deveria ocorrer em 15 de fevereiro. Foto mostra seringas com rótulos laranja para aplicação da vacina da Pfizer em crianças de 5 a 11 anos em Chicago, nos Estados Unidos, no dia 11 de dezembro.
Nam Y. Huh/AP
A agência reguladora dos Estados Unidos (FDA, sigla em inglês) adiou a avaliação sobre a liberação da vacina da Pfizer para crianças com menos 5 anos e disse, nesta sexta-feira (11), que aguarda novos dados sobre a eficácia do imunizante na faixa etária.
Em nota, a FDA informou que recebeu uma notificação da Pfizer sobre novos dados que surgiram recentemente, e que são relevantes para a solicitação de autorização para o uso emergencial da vacina em crianças com idades de 6 meses a 4 anos.
“Como parte de sua submissão contínua, a empresa notificou recentemente a agência sobre descobertas adicionais de seu ensaio clínico em andamento”, disse a agência. A submissão contínua é um modelo que permite que as farmacêuticas continuem enviando dados no decorrer do processo, uma forma de aumentar a agilidade para a análise e garantir uma aprovação mais rápida em tempos de pandemia.
Com a decisão, a agência dos EUA disse que está adiando uma reunião prevista para 15 de fevereiro, que originalmente teria o papel de decidir sobre o assunto.
“Isso dará à agência tempo para considerar os dados adicionais, permitindo uma discussão pública transparente como parte de nossos processos científicos e regulatórios usuais para vacinas para a Covid-19”.
Fonte: G1 Mundo